Øjensygdomme skyldes fejl i ’antenner’ på cellernes overflade
Vores evne til at se afhænger af lysfølsomme sanseceller i øjets nethinde. Forskere fra blandt andre Københavns Universitet har nu afdækket den komplekse molekylære mekanisme bag sygdomme, som skyldes fejl i sansecellernes antennestrukturer.
Øjets sanseceller kan deles op i dagslysceller (tappe) og natlysceller (stave). Både tappe og stave består af et indre segment, hvor al cellens proteinsyntese foregår, samt et ydre segment, der indeholder cellens lysfølsomme pigmenter. Under øjets udvikling dannes det ydre segment ud fra det primære cilie, som er en antenne-lignende struktur på celleoverfladen. Tidligere studier har vist, at mutationer i genet, det koder for proteinet CEP78, giver ophav til en speciel type øjensygdom karakteriseret ved stav- og tap dystrofi samt hørenedsættelse. Den molekylære mekanisme bag disse sygdomme har imidlertid indtil nu været ganske ukendt.
I et nyt studie viser forskere fra Biologisk Institut, Københavns Universitet sammen med forskere fra Syddansk Universitet og universiteter i udlandet, at mutationer i et helt bestemt gen - nemlig CEP78 genet - både hæmmer cellernes evne til at danne de primære cilier, samt bevirker at de få cilier, der dannes på cellerne, bliver alt for lange.
- ”Det allervigtigste vi har fundet ud af er, at CEP78 regulerer ciliedannelsen ved at aktivere en såkaldt ubiquitin ligase, der stimulerer nedbrydningen af proteinet CP110, når cilier udvikles. Vores studie viser, at CEP78 spiller en helt central rolle for fjernelsen af CP110 og dermed initiering af ciliedannelsen”, udtaler Professor Lotte Bang Pedersen, som har ledet projektet.
- Lotte Bang Pedersen forklarer endvidere: ”Udover at påvise en central rolle for CEP78 i fjernelsen af CP110, har vi i vores studie afdækket en ny sammenhæng mellem CEP78 og et tredje protein, CEP350. Vi vidste allerede fra andre studier, at CEP350 var vigtigt for ciliedannelsen, men nu viser vi, at CEP350 sørger for et samspil med CEP78, således at CP110 kan blive fjernet under initiering af ciliogenesen. Mekanismen, hvorved CEP78 regulerer ciliets længde, er endnu uklar, men vores resultater tyder på, at CEP350 - og ikke CP110 - kan være involveret i denne proces.”
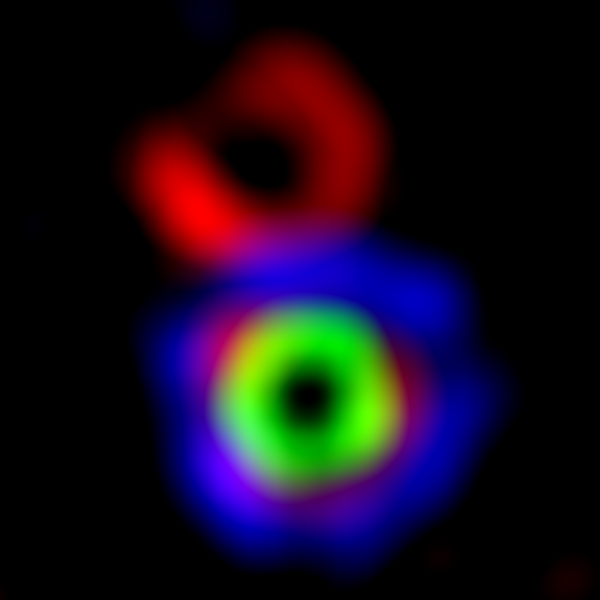
- ”Eftersom stav- og tapcellernes ydre segmenter dannes ud fra primære cilier forklarer vores resultater, hvorfor patienter med mutationer i CEP78 genet udvikler stav- og tap dystrofi. Hårcellerne i det indre øre, som er ørets sanseceller, der opfanger lyd, indeholder tilsvarende et enkelt primært cilie, som er vigtigt for dannelsen og funktionen af hårcellerne. Således kan vores resultater også forklare, hvorfor patienter med mutationer i CEP78 genet lider af hørenedsættelse”, fortsætter Lotte Bang Pedersen.
På sigt kan resultaterne få betydning for diagnose og behandling af patienter med øjensygdomme og hørenedsættelse, Det er blandt andet helt oplagt fremover at inkludere CEP350 som muligt sygdomsgen ved genetisk screening af patienter med disse sygdomme.
Kontakt
Professor Lotte Bang Pedersen
Sektion for Cellebiologi- og Fysiologi
Biologisk Institut
Tlf. +45 2980 3551
Mail: lbpedersen@bio.ku.dk
Sidsel Kretzschmer Henriksen
Presse og kommunikation
Biologisk Institut
Tlf. +45 3533 4147
Mail: sidsel.henriksen@bio.ku.dk
Helle Blæsild
Teamleder, PR & Kommunikation
Biologisk Institut
Tlf. +45 2875 2076
Mail: helleb@bio.ku.dk

